Entrez un mot ou une phrase dans n'importe quelle langue 👆
Langue:
Traduction et analyse de mots par intelligence artificielle ChatGPT
Sur cette page, vous pouvez obtenir une analyse détaillée d'un mot ou d'une phrase, réalisée à l'aide de la meilleure technologie d'intelligence artificielle à ce jour:
- comment le mot est utilisé
- fréquence d'utilisation
- il est utilisé plus souvent dans le discours oral ou écrit
- options de traduction de mots
- exemples d'utilisation (plusieurs phrases avec traduction)
- étymologie
Qu'est-ce (qui) est Гемоглобин - définition
ГРУППА ЖЕЛЕЗОСОДЕРЖАЩИХ БЕЛКОВ ЖИВОТНЫХ, КОТОРЫЕ ОБЕСПЕЧИВАЮТ ПЕРЕНОС КИСЛОРОДА В ТКАНИ
Метгемоглобин; Гемоглобины; Оксигемоглобин; Метагемоглобин; Hb
ГЕМОГЛОБИН
(от гемо ... и лат. globus - шар), красный дыхательный пигмент крови человека, позвоночных и некоторых беспозвоночных животных. Состоит из белка (глобина) и железопорфирина - гема. Переносит кислород от органов дыхания к тканям и углекислый газ от тканей к дыхательным органам. У различных видов организмов гемоглобин имеет разное строение. Многие заболевания крови (анемии) связаны с нарушениями строения гемоглобина, в т. ч. наследственными.
гемоглобин
м.
Красный железосодержащий пигмент крови, осуществляющий перенос кислорода из легких в ткани организма.
Красный железосодержащий пигмент крови, осуществляющий перенос кислорода из легких в ткани организма.
Гемоглобин
(Hb)
(от гемо... (См. Гемо...) и лат. globus - шар), красный железосодержащий пигмент крови человека, позвоночных и некоторых беспозвоночных животных; в организме выполняет функцию переноса кислорода (O2) из органов дыхания к тканям; играет также важную роль в переносе углекислого газа от тканей в органы дыхания. У большинства беспозвоночных Г. свободно растворён в крови; у позвоночных и некоторых беспозвоночных находится в красных кровяных клетках - эритроцитах, составляя до 94\% их сухого остатка. Молярная масса Г., включенного в эритроциты, около 66 000, растворённого в плазме - до 3000000. По химической природе Г. - сложный белок - хромопротеид (См. Хромопротеиды), состоящий из белка глобина и железопорфирина - гема. У высших животных и человека Г. состоит из 4 субъединиц-мономеров с молярной массой около 17000; два мономера содержат по 141 остатку аминокислот (α-цепи), два других - по 146 остатков (β-цепи).
Пространственные структуры этих полипептидов во многом аналогичны. Они образуют характерные "гидрофобные карманы", в которых размещены молекулы гема (по одной на каждую субъединицу). Из 6 координационных связей атома железа, входящего в состав гема, 4 направлены на азот пиррольных колец; 5-я соединена с азотом имидазольного кольца гистидина, принадлежащего полипептидам и стоящего на 87-м месте в α-цепи и на 92-м месте в β-цепи; 6-я связь направлена на молекулу воды или др. группы (лиганды) и в том числе на кислород. Субъединицы рыхло связаны между собой водородными, солевыми и др. нековалентными связями и легко диссоциируют под влиянием амидов, повышенной концентрации солей с образованием главным образом симметричных димеров (αβ) и частично α- и β-мономеров. Пространственная структура молекулы Г. изучена методом рентгеноструктурного анализа (М. Перуц, 1959).
Последовательность расположения аминокислот в α- и β-цепях Г. ряда высших животных и человека полностью выяснена. В собранной в тетрамер молекуле Г. все 4 остатка гема расположены на поверхности и легко доступны реакции с O2. Присоединение O2 обеспечивается содержанием в геме атома Fe2+. Эта реакция обратима и зависит от парциального давления (напряжения) O2. В капиллярах лёгких, где напряжение O2 около 100 мм рт. ст., Г. соединяется с O2 (процесс оксигенации), превращаясь в оксигенированный Г. - оксигемоглобин. В капиллярах тканей, где напряжение O2 значительно ниже (ок. 40 мм рт. ст.), происходит диссоциация оксигемоглобина на Г. и O2; последний поступает в клетки органов и тканей, где парциальное давление O2 ещё ниже (5-20 мм рт. cm.); в глубине клеток оно падает практически до нуля. Присоединение O2 к Г. и диссоциация оксигемоглобина на Г. и O2 сопровождаются конформационными (пространственными) изменениями молекулы Г., а также его обратимым распадом на димеры и мономеры с последующей агрегацией в тетрамеры.
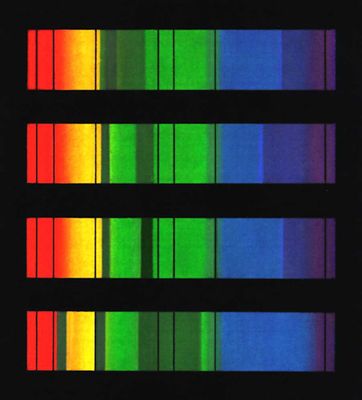
Изменяются при реакции с O2 и др. свойства Г.: оксигенированный Г. - в 70 раз более сильная кислота, чем Г. Это играет большую роль в связывании в тканях и отдаче в лёгких CO2. Характерны полосы поглощения в видимой части спектра: у Г. - один максимум (при 554 ммк), у оксигенированного Г. - два максимума при 578 и 540 ммк. Г. способен непосредственно присоединять CO2 (в результате реакции CO2 с NH2-rpyппами глобина); при этом образуется карбгемоглобин - соединение неустойчивое, легко распадающееся в капиллярах лёгких на Г. и CO2.
Количество Г. в крови человека - в среднем 13-16 г\% (или 78\%-96\% по Сали); у женщин Г. несколько меньше, чем у мужчин. Свойства Г. меняются в онтогенезе. Поэтому различают Г. эмбриональный, Г. - плода (foetus) - HbF, Г. взрослых (adult) - HbA. Сродство к кислороду у Г. плода выше, чем у Г. взрослых, что имеет существенное физиологическое значение и обеспечивает большую устойчивость организма плода к недостатку O2. Определение количества Г. в крови имеет важное значение для характеристики дыхательной функции крови в нормальных условиях и при самых различных заболеваниях, особенно при болезнях крови. Количество Г. определяют специальными приборами - гемометрами.
При некоторых заболеваниях, а также при врождённых аномалиях крови (см. Гемоглобинопатии) в эритроцитах появляются аномальные (патологические) Г., отличающиеся от нормальных замещением аминокислотного остатка в (- или β-цепях. Выделено более 50 разновидностей аномальных Г. Так, при серповидноклеточной анемии обнаружен Г., в β-цепях которого глутаминовая кислота, стоящая на 6-м месте от N-koнца, замещена валином. Аномалии эритроцитов, связанные с содержанием гемоглобина F или Н, лежат в основе талассемии (См. Талассемия), метгемоглобинемии (См. Метгемоглобинемия). Дыхательная функция некоторых аномальных Г. резко нарушена, что обусловливает различные патологические состояния (анемии (См. Анемия) и др.). Свойства Г. могут меняться при отравлении организма, например угарным газом, вызывающим образование Карбоксигемоглобина, или ядами, переводящими Fe2+ гема в Fe3+ с образованием метгемоглобина. Эти производные Г. не способны переносить кислород. Г. различных животных обладают видовой специфичностью, обусловленной своеобразием строения белковой части молекулы. Г., освобождающийся при разрушении эритроцитов, - источник образования жёлчных пигментов (См. Жёлчные пигменты).
В мышечной ткани содержится мышечный Г. - Миоглобин, по молярной массе, составу и свойствам близкий к субъединицам Г. (мономерам). Аналоги Г. обнаружены у некоторых растений (например, Леггемоглобин содержится в клубеньках бобовых).
Лит.: Коржуев П. А., Гемоглобин, М., 1964; Гауровиц Ф., Химия и функции белков, пер. с англ., 2 изд., М., 1965, с. 303-23; Ингрэм В., Биосинтез макромолекул, пер. с англ., М., 1966, с. 188-97; Рапопорт С. М., Медицинская биохимия, пер. с нем., М., 1966; Перутц М., Молекула гемоглобина, в сборнике: Молекулы и клетки, М., 1966; Цукеркандль Э.; Эволюция гемоглобина, там же; Fanelli A. R., AntoniniE., Caputo A., Hemoglobin and myoglobin, "Advances in Protein Chemistry", 1964, v. 19, p. 73-222; Antonini Е., Brunori M., Hemoglobin, "Annual Review of Biochemistry", 1970, v. 39, p. 977-1042.
Г. В. Андреенко, С. Е. Северин.

Спектры поглощения гемоглобина и его соединений: 1 - гемоглобин; 2 - оксигемоглобин; 3 - карбоксигемоглобин; 4 - метгемоглобин: B, C, D, E, F, G - основные фраунгоферовы линии солнечного спектра, цифрами обозначены длины волн.
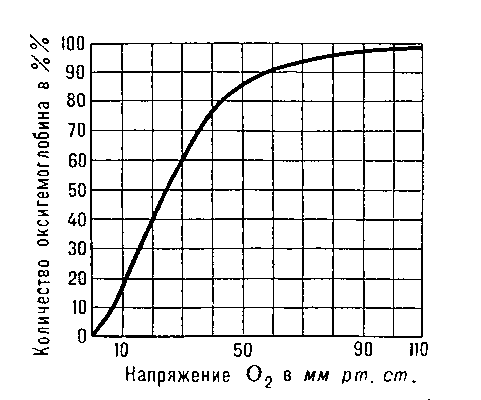
Кривая диссоциации оксигемоглобина человека.
Wikipédia
Гемоглобин

Гемоглоби́н (от др.-греч. αἷμα «кровь» + лат. globus «шар») (Hb или Hgb) — сложный железосодержащий белок животных, обладающих кровообращением, способный обратимо связываться с кислородом, обеспечивая его перенос в ткани. У позвоночных животных содержится в эритроцитах, у большинства беспозвоночных растворён в плазме крови (эритрокруорин) и может присутствовать в других тканях. Молекулярная масса гемоглобина человека — около 66,8 кДа. Молекула гемоглобина может нести до четырёх молекул кислорода. Один грамм гемоглобина может переносить до 1,34 мл кислорода.
Exemples du corpus de texte pour Гемоглобин
1. Низкий гемоглобин - это нескончаемая изнурительная слабость, анемичность.
2. Голос крови "Красная кровь": гемоглобин, эритроциты, гематокрит.
3. Гемоглобин у меня всегда маленький, беспокоиться нечего.
4. Гемоглобин в организме человека играет огромную роль.
5. Например, синтетический гемоглобин или гормоны роста.






